Хром
Хром (Cr), химический элемент VI группы периодической системы Менделеева. Относится к переходным металлом с атомным номером 24 и атомной массой 51,996. В переводе с греческого, название металла означает «цвет». Такому названию металл обязан разнообразной цветовой гамме, которая присуща его различным соединениям.

Физические характеристики хрома
Металл обладает достаточной твердостью и хрупкостью одновременно. По шкале Мооса твердость хрома оценивается в 5,5. Этот показатель означает, что хром имеет максимальную твердость из всех известных на сегодня металлов, после урана, иридия, вольфрама и бериллия. Для простого вещества хрома характерен голубовато-белый окрас.
| Атомный номер | 24 |
| Атомная масса | 51,996 |
| Плотность, кг/м³ | 7190 |
| Температура плавления, °С | 1856 |
| Теплоемкость, кДж/(кг·°С) | 0,46 |
| Электроотрицательность | 1,6 |
| Ковалентный радиус, Å | 1,18 |
| 1-й ионизац. потенциал, эв | 6,76 |
Металл не относится к редким элементам. Его концентрация в земной коре достигает 0,02% масс. долей. В чистом виде хром не встречается никогда. Он содержится в минералах и рудах, которые являются главным источником добычи металла. Хромит (хромистый железняк, FeO*Cr2O3) считается основным соединением хрома. Еще одним достаточно распространенным, однако менее важным минералом, является крокоит PbCrO4.
Металл легко поддается плавке при температуре 19070С (21800К или 34650F). При температуре в 26720С – закипает. Атомная масса металла составляет 51,996 г/моль.
Хром является уникальным металлом благодаря своим магнитным свойствам. В условиях комнатной температуры ему присуще антиферромагнитное упорядочение, в то время, как другие металлы обладают им в условиях исключительно пониженных температур. Однако, если хром нагреть выше 370С, физические свойства хрома изменяются. Так, существенно меняется электросопротивление и коэффициент линейного расширения, модуль упругости достигает минимального значения, а внутреннее трение значительно увеличивается. Такое явление связано с прохождением точки Нееля, при которой антиферромагнитные свойства материала способны изменяться на парамагнитные. Это означает, что первый уровень пройден, и вещество резко увеличилось в объеме.
Строение хрома представляет собой объемно-центрированную решетку, благодаря которой металл характеризуется температурой хрупко-вязкого периода. Однако, в случае с данным металлом, огромное значение имеет степень чистоты, поэтому, величина находится в пределах -500С - +3500С. Как показывает практика, раскристаллизированный металл не имеет никакой пластичности, но мягкий отжиг и формовка делают его ковким.
Химические свойства хрома
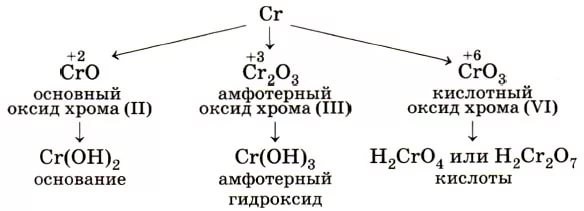
Атом имеет следующую внешнюю конфигурацию: 3d54s1. Как правило, в соединениях хром имеет следующие степени окисления: +2, +3, +6, среди которых наибольшую устойчивость проявляет Сr3+.Кроме этого существуют и другие соединения, в которых хром проявляет совершенно иную степень окисления, а именно: +1, +4, +5.
Металл не отличается особой химической активностью. Во время нахождения хрома в обычных условиях, металл проявляет устойчивость к влаге и кислороду. Однако, данная характеристика не относится к соединению хрома и фтора – CrF3, которое при воздействии температур, превышающих 6000С, взаимодействует с парами воды, образуя в результате реакции Сr2О3, а также азотом, углеродом и серой.
Во время нагревания металлического хрома, он взаимодействует с галогенами, серой, кремнием, бором, углеродом, а также некоторыми другими элементами, в результате чего получаются следующие химические реакции хрома:
Cr + 2F2 = CrF4 (с примесью CrF5)
2Cr + 3Cl2 = 2CrCl3
2Cr + 3S = Cr2S3
Хроматы можно получить, если нагреть хром с расплавленной содой на воздухе, нитратами или хлоратами щелочных металлов:
2Cr + 2Na2CO3 + 3O2 = 2Na2CrO4 + 2CO2.
Хром не обладает токсичностью, чего нельзя сказать о некоторых его соединениях. Как известно, пыль данного металла, при попадании в организм, может раздражать легкие, через кожу она не усваивается. Но, поскольку в чистом виде он не встречается, то его попадание в человеческий организм является невозможным.
Трехвалентный хром попадает в окружающую среду во время добычи и переработки хромовой руды. В человеческий организм попадание хрома вероятно в виде пищевой добавки, используемой в программах по похудению. Хром с валентностью, равной +3, является активным участником синтеза глюкозы. Ученые установили, что излишнее употребление хрома особого вреда человеческому организму не наносит, поскольку не происходит его всасывание, однако, он способен накапливаться в организме.
Соединения, в котором участвует шестивалентный металл, являются крайне токсичными. Вероятность их попадания в человеческий организм появляется во время производства хроматов, хромирования предметов, во время проведения некоторых сварочных работ. Попадание такого хрома в организм чревато серьезными последствиями, так как соединения, в которых присутствует шестивалентный элемент, представляют собой сильные окислители. Поэтому, могут вызвать кровотечение в желудке и кишечнике, иногда с прободением кишечника. При попадании таких соединений на кожу возникают сильные химические реакции в виде ожогов, воспалений, возникновения язв.
В зависимости от качества хрома, которое необходимо получить на выходе, существует несколько способов производства металла: электролизом концентрированных водных растворов оксида хрома, электролизом сульфатов, а также восстановлением оксидом кремния. Однако, последний способ не очень популярен, так как при нем на выходе получается хром с огромным количеством примесей. Кроме того, он также является экономически невыгодным.
| Степень окисления | Оксид | Гидроксид | Характер | Преобладающие формы в растворах | Примечания |
| +2 | CrO (чёрный) | Cr(OH)2 (желтый) | Основный | Cr2+ (соли голубого цвета) | Очень сильный восстановитель |
|
+3 |
Cr2O3 (зелёный) | Cr(OH)3 (серо-зеленый) | Амфотерный |
Cr3+ (зеленые или лиловые соли) |
|
| +4 | CrO2 | не существует | Несолеобразующий | - |
Встречается редко, малохарактерна |
| +6 | CrO3 (красный) |
H2CrO4 |
Кислотный |
CrO42- (хроматы, желтые) |
Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. |
 Горная промышленность
Горная промышленность
Полиция Венгрии выдала ордер на арест 21?летнего уроженца Сайтамы, известного в СМИ как Suzuki George, как подозреваемого в краже значительной суммы из епархиального дома Венгерской православной епархии в Будапеште.
Он из города Сайтама (Япония), август 2002, и был объявлен в розыск в конце января 2024.
Епархия Венгерская и Будапештская РПЦ, по данным РИА Новости, не раскрывает содержимое похищенного, и не комментирует личность подозреваемого, чтобы не влиять на ход следствия.
<u><b>Our swift action</b></u> - some solution at reducing thy expenses with any ensuing extensive fixes!
<a href=https://5.gp/b31q6i3y><b>Try our swiftness plus standard among help right now!</b></a>
Thought I’d drop this here, I visited this site recently: <a href=https://maba-3d-druck.de>relevant too</a>
Feel free to comment.
Документ максимально приближен к оригиналу и проходит визуальную проверку.
Мы гарантируем, что в случае проверки документа, подозрений не возникнет.
- Конфиденциально
- Доставка 3–7 дней
- Любая специальность
Уже более 2472 клиентов воспользовались услугой — теперь ваша очередь.
<a href=http://spbrcom31.ru/>Купить дипломы о высшем</a> — ответим быстро, без лишних формальностей.
Джубга — популярное место для отдыха на Черноморском побережье. Здесь особенно приятно проводить летние дни на пляже, наслаждаясь тёплым солнцем.
На Джубге туристы могут насладиться яркими развлечениями и комфортным жильем. Гостеприимные владельцы готовы предложить своим гостям уютные номера и демократичные цены.
Береговая линия Джубги предлагает отдыхающим прекрасные пляжи с чистым морем. Для любителей активного отдыха доступны различные водные аттракционы и экскурсии.
Особое внимание в Джубге стоит уделить местной кухне. Местные рестораны славятся своим вкусным меню, включающим морепродукты и национальные блюда.
джубга снять жилье <a href=https://otdyh-dzhubga1.ru/>джубга снять жилье</a> .
The concept of a drone light show represents a cutting-edge form of entertainment. These aerial displays combine technology and artistry to create stunning visuals in the night sky.
Versatility is one of the significant benefits of using drones for light shows. They can be customized to fit any event, whether it be a wedding or a public celebration.
The ecological footprint of these aerial displays is another critical consideration. Drones do not produce harmful emissions like fireworks do, making them a greener alternative.
As technology continues to evolve, the future of drone light shows looks promising. In the years to come, we are likely to witness increasingly elaborate and coordinated displays.
Apple – один из ведущих брендов в области технологий. Apple выпускает разнообразные товары, начиная от iPhone и заканчивая iPad и Mac.
Одним из ключевых факторов успеха Apple является инновационный дизайн. Apple всегда нацелена на повышения удобства пользования и функциональности своих товаров.
Кроме того, экосистема Apple создает уникальный опыт для пользователей. Устройства компании легко интегрируются друг с другом, что делает использование их еще проще.
Хотя цены на продукцию Apple могут быть высокими, они все равно пользуются популярностью. Покупатели предпочитают продукты Apple за их высокое качество, надежность и использование современных технологий.
<a href=https://evomedlabs.com/>cialis online</a>
<a href=https://vantagecoremed.com/>cialis for women</a>