Тяжелые металлы
На сегодняшний день известно порядка 40 различных трактовок термина «тяжелые металлы», и совершенно невозможно выделить одну наиболее правильную. Так, каждое определение тяжелых металлов будет включать свой перечень элементов согласно с теми или иными критериями. Зачастую характеристика тяжелых металлов основывается на: атомной массе, плотности, токсичности, распространенности в природной среде, степени вовлеченности в природные и техногенные циклы. Например, основным критерием может являться минимальная относительная атомная масса, равная 50. Согласно данной особенности, под список «тяжелых металлов» попадут абсолютно все металлы, начиная с ванадия, вне зависимости от их плотности. Однако, в других определениях данного термина именно плотность является главной характеристикой, на основе которой и составляется перечень, и она должна быть более или равной 8 г/см3 (плотность железа). Согласно данному критерию в список «тяжелых металлов» будут включены следующие элементы: свинец, ртуть, медь, кадмий, кобальт, а вот олово уже будет исключено из данного списка, так оно более легкое. Кроме того, также в основе классификации металлов могут находится и другие значения пороговой плотности (например, в 5 г/см3) или атомной массы. Таким образом, к некоторым группа тяжелых металлов могут попадать элементы, которые являются хрупкими или металлоидами (например, висмут или мышьяк, соответственно). В связи с этим, термин «тяжелые металлы» рассматривается с медицинской и природоохранной точек зрения. Это позволяет при составлении списка тяжелых металлов основываться не только на физических и химический свойствах элемента, но и на его биологической активности, токсичности, а также объеме его применения в хозяйственной деятельности.
Однако, все же в большинстве случаев, в список тяжелых металлов входит 40 элементов, имеющие относительную плотность, превышающую 6. Не смотря на то, что термин «тяжелые металлы» и «токсичные металлы» принято считать синонимами, все же количество опасных металлов существенно меньше, что не может не радовать.
В первую очередь интерес представляют элементы, имеющие самое широкое и активное использование в производстве, в результате чего происходит их накопление в окружающей среде, что и представляет опасность здоровью человечества с точки зрения их биологической активности и токсичности. Среди таковых следует выделить свинец, ртуть, кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьму, ванадий, марганец, хром, молибден и мышьяк.
Свойства тяжелых металлов
Тяжелые металлы в атмосфере представляют собой органические и неорганические соединения. Они могут присутствовать как пыль, аэрозоль, или же иметь газообразную элементную форму (например, ртуть). Стоит отметить, что свинец, кадмий, медь и цинк в виде аэрозоля включают в себя, главным образом, субмикронные частицы, диаметр которых составляет примерно 0,5 – 1 мкм. А вот частицы никеля и кобальта в виде аэрозоля представляют собой крупнодисперсные частицы, имеющие диаметр, превышающий 1 мкм. Их образование, в основном, происходит во время сгорания дизельного топлива.
В водной среде тяжелые металлы могут быть представлены в виде трех основных форм: взвешенных частиц, коллоидных частиц, а также растворенных соединений. Последние представляют собой свободные ионы и растворимые комплексные соединения с органическими (гуминовые и фульвокислоты) и неорганическими (галогены, сульфаты, фосфаты, карбонаты) лигандами. Форма нахождения элемента в воде определяется гидролизом, который очень сильно влияет на нахождение указанных элементов в водной среде. Огромное количество тяжелых металлов переносится посредством поверхностных вод во взвешенном состоянии.
Содержание тяжелых металлов в почвах представлено водорастворимой, ионообменной и непрочно адсорбированной формах. Первые, главным образом, представляют собой хлориды, нитраты, сульфаты, а также органические комплексные соединения. Следует сказать, что часто отмечается связь ионов тяжелых металлов с минералами почвы, как часть кристаллической решетки.
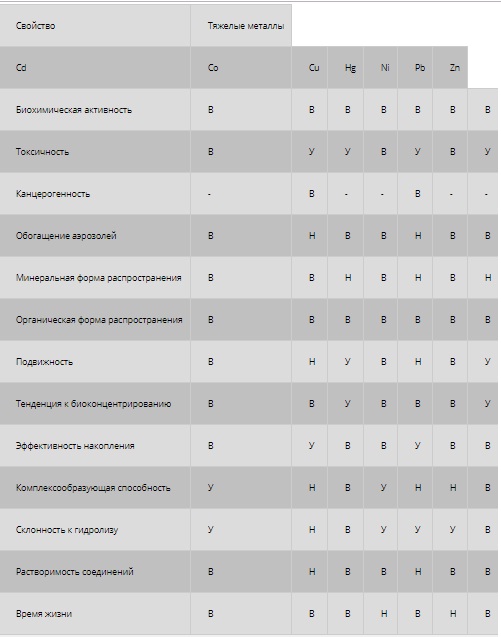
В таблице представлены биогеохимические свойства тяжелых металлов, оценка которых осуществлялась по трем главным критериям: высокая (В), умеренная (У), низкая (Н).
Стоит отметить, что к биогеохимическим свойствам тяжелых металлов относятся токсичность, канцерогенность, растворимость и многие другие, которые выражены у них по-разному. Однако, существует два основных свойства, на основе которых и определяется степень опасности того или иного тяжелого металла для живого организма в зависимости от концентрации. К данным свойствам относятся: биохимическая активность и органическая форма распространения.
Определение тяжелых металлов
На сегодняшний день есть две главные группы аналитических методов, которые позволяют определять тяжелые металлы (например, в воде или почве), а именно:
- электрохимические методы;
- спектрометрические методы.
Стоит отметить что вторая группа постепенно сдает свои позиции и уступает электрохимическим методам.

Среди спектрометрических методов следует выделить наиболее распространенный – атомно-абсорбционную спектрометрию с разной атомизацией образцов. В том случае, когда необходимо определить несколько элементов одновременно, главным методом определения выступают атомная эмиссионная спектрометрия с индукционно связанной плазмой, а также масс-спектрометрия с индукционно связанной плазмой.
Для того, чтобы определить тяжелые металлы электрохимическими способами пробу переводят в водный раствор. К электрохимическим методам относятся: полярографический (вольтамперометрический), потенциометрический, кулонометрический, кондуктометрический и многие другие. Стоит отметить, что бывают ситуации, когда невозможно определить тяжелые металлы с помощью лишь только одного метода, тогда используются сразу несколько методов с дальнейшим титрованием. Данные методы основываются на анализе вольт-амперных характеристик, потенциалов ион-селективных электродов, интегрального заряда, который служит для того, чтобы искомый метал выпал в осадок на электроде электрохимической ячейке, электропроводности раствора и т.д. Указанные способы позволяют определять тяжелые металлы до 10-9 моль/л.
Группа спектральных анализов является включает в себя множество различных методов, с помощью которых осуществляется определение тяжелых металлов. Прежде всего, она включает в свой перечень атомный эмиссионный анализ, атомный абсорбционный анализ, спектрофотометрию, масс-спектрометрию, спектрометрию с индуктивно связанной плазмой, рентгеноспектральный анализ.
В отдельных случаях, когда концентрация тяжелых металлов находится в достаточно небольшой концентрации, то они определяются, зачастую, несколькими методами спектрометрии.
Иногда, для определения тяжелых металлов, следует прибегнуть к комплексным методам, которые сочетают в себе как спектральные, как и электрохимические способы. Одним из таких методов является спектрополяриметральный анализ.
Самый тяжелый металл
Определить и назвать один единственный самый тяжелый металл невозможно, так как критерии определения «тяжести» металла могут быть совершенно разными. Об этом шла речь в начале данной статьи. Таким образом, одним из самых тяжелых металлов является свинец, которому не уступают цинк, олово, железо, и медь, однако он не может носить титул самого тяжелого металла. Например, свинец существенно уступает жидкому металлу – ртути. Так, если поместить в ртуть кусочек свинца, то он не утонет, а будет уверенно держаться на ее поверхности. Бутылка с ртутью объемом в 1 литр будет весить 14 кг. Но, не смотря на это, и ртуть не является самым тяжелым металлом, так как золото и платина тяжелее ртути в полтора раза.
Опережают золото и платину редкие металлы – иридий и осмий, которые в два раза тяжелее железа. Итак, самые тяжелые металлы, согласно их удельному весу:
- цинк – 7,1;
- олово – 7,3;
- железо – 7,8;
- медь – 8,9;
- свинец – 11,3;
- ртуть – 13,6;
- золото – 19,3;
- платина – 21,5;
- иридий – 22,4;
- осмий – 22,5
Если же взять за основную характеристику тяжелых металлов плотность, то список будет отличаться, и в него войдут следующие элементы:
- тантал – 16,67 г/см3;
- уран – 19,05 г/см3;
- вольфрам – 19,29 г/см3;
- золото – 19,29 г/см3;
- плутоний – 19,80 г/см3;
- нептуний – 20,47 г/см3;
- рений – 21,01 г/см3;
- платина – 21,40 г/см3;
- осмий – 22,61 г/см3;
- иридий – 22,65 г/см3;
Однако, существует перечень металлов, которых общепринято считать тяжелыми. Основные тяжелые металлы:
- свинец;
- ртуть;
- медь;
- кадмий;
- кобальт.
Особенности тяжелых металлов заключаются в том, что все они обладают высокой токсичностью и в некоторых случаях несут угрозу здоровью и жизни живых организмов. Кроме этого, они обладают способностью к биоаккумуляции и биомагнификации.
Применение тяжелых металлов
В далекие времена появившиеся первые металлы в жизни человека существенно облегчили его существование на Земле. Ведь металл является более прочным материалом, чем камень или дерево. Из металла получались более продуктивные орудия труда, более разрушительное оружие, а также более надежная защита. Кроме этого, из металла люди также научились изготавливать украшения, посуду, различные ритуальные предметы, а также предметы повседневного обихода. На сегодняшний день человечеству известно порядка 70 металлов, часть из которых, согласно разным определениям и критериям отбора, являются тяжелыми. Благодаря своим уникальным свойствам и особенностям, тяжелые металлы нашли свое применение во многих сферах человеческой деятельности, в частности, в машиностроении, судостроении, авиастроении, медицине, производстве техники и электроники, строительстве, в производстве посуды, украшений, а также вещей повседневного обихода.

Например, свинец используется для покрытия различной аппаратуры с целью ее защиты от коррозии. Также его используют в качестве оболочки кабелей, которые прокладываются под землей, в воде или любой другой влажной среде. Для зажигания двигателей внутреннего сгорания все так же используются свинцовые аккумуляторы, не смотря на то, что уже в природе давно существуют никелевые аккумуляторы, однако, стоимость последних значительно выше.
Ртуть также нашла свое широкое применение в электротехнике, электронике, приборостроении, металлургии, химии (изготовление термометров, барометров, реле, лампы дневного света, кварцевые ртутные лампы) и т.д.
Медь благодаря своему низкому удельному сопротивлению и высокой теплопроводности, достаточно широко используется в электротехнике – она является основным материалом, из которого производят силовые и другие кабели, провода, другие проводники. Из меди изготавливают различные теплообменники – радиаторы охлаждения, кондиционирования, отопления, компьютерные кулеры, тепловые трубки и многое другое.
Данные элементы добываются из руды тяжелых металлов – изначально извлекается руда, после чего осуществляется ее обогащение и затем при помощи химического или электролитического восстановления уже получается сам металл.
 Горная промышленность
Горная промышленность
<a href=http://datingsitesover.com/?>online free dating service </a>
speed dating in the dark gay
<a href=http://gaychatgay.com?>gay dating culture canada</a>
gay christian dating services
<a href=http://gaydatingzz.com?>white men gay dating site</a>
serious gay dating websites
<a href=http://gaychatgay.com?>gay dating asian guys daddy</a>
top gay dating sites 2021
<a href=http://freegaychatnew.com?>free gay dating siyte</a>
best friend is gay dating
<a href=http://gaychatrooms.org?>top gay dating sites 2021</a>
joe lozano l gay dating
<a href=http://freegaychatnew.com?>gay older dating</a>
spanish gay dating site
<a href=http://freegaychatnew.com?>gay thai dating</a>
gay dating culture canada
<a href=http://gaychatgay.com?>married gay dating</a>
gay speed dating nyc 2021
<a href=http://gayonlinedating.net?>gay bbw men dating michigan</a>
gay dating houston texas
<a href=http://datinggayservices.com/?>gay online dating art</a>
<a href=https://essayghostwriter.com/?>top resume writing services</a>
<a href=https://essaypoints.com/?>custom essay writing service</a>
<a href=https://essaypoints.com/?>help with my essay</a>
<a href=https://buy1essay.com/?>write a personal essay</a>
write college essays for money
<a href=https://essayprepworkshop.com/?>how to conclude an argumentative essay</a>
500 word essay
<a href=https://cybersexgames.net/?>free 3d adult sex games</a>
sex question games
<a href=https://cybersexgames.net/?>sex games for android</a>
sex games hacked
<a href=https://sex4games.com/?>games of thrones sex scenes</a>
character customization sex games
<a href=https://sex4games.com/?>free sex games for adults</a>
sex games for ios
<a href=https://sex4games.com/?>childhood sex games</a>
games of thrines sex scences
<a href=https://sexgamesx.net/?>sex online games</a>
offline sex games
<a href=https://ketogenicdiets.net/?>are blueberries keto</a>
snacks on keto diet
<a href=https://ketogendiets.com/?>keto pills review</a>
the diet doctor keto
<a href=https://sexygamess.com/?>college rules sex games</a>
custom hero sex games
<a href=https://winsexgames.com/?>sex trivia games</a>
couples play games blindfolded sex
<a href=https://sex4games.com/?>free interactive sex games</a>
sex games phone
<a href=https://sexgameszone.com/?>crazy sex games</a>
animated fucktown sex games
<a href=https://sexygamess.com/?>mature tv sex show games</a>
lesbian shower sex games
<a href=https://buy1essay.com/?>college essay writing</a>
pay someone to write my essay
<a href=https://multiessay.com/?>wriВte an anaВlyВsis essay</a>
english essay writing
<a href=https://casinoonlinet.com/?>writing college essays for money</a>
writing a response essay
<a href=https://onlinecasinoad.com/?>essay writing books</a>
writing a comparative essay
<a href=https://casinoonlinek.com/?>the write stuff thinking through essays</a>
help writing essay
<a href=https://checkyouressay.com/?>mla format example essay</a>
help me write my essay
<a href=https://dollaressays.com/?>college essay format example</a>
essay on unions
<a href=https://addonsvpn.com>best vpn service for mac</a>
what is vpn?
<a href=https://choosevpn.net>vpn best buy</a>
completely free vpn
<a href=https://essayscratch.com>how many words should an essay be</a>
illustration essay
<a href=https://essaysitesreviews.com>nhs essay examples</a>
how to cite in an essay
<a href=https://gay-buddies.com>western pa gay chat</a>
gay chat on webcam
<a href=https://gaytgpost.com/>gay chat sex</a>
gay chat rpulete
<a href=https://ketogendiet.net/>dr axe keto diet</a>
keto diet bad for you
<a href=https://ketogendiets.com/>keto diet meal planner</a>
keto diet how to
<a href=https://ketogenicdietinfo.com/>dr oz keto diet</a>
keto diet list
<a href=https://ketogenicdiets.net/>what's keto diet</a>
fruit for keto diet
<a href=https://thebestvpnpro.com/>hola vpn</a>
uf health vpn
<a href=https://tjvpn.net/>free vpn canada</a>
best chrome vpn free
<a href=https://topessayswriter.com/>essay service</a>
essay writing format
<a href=https://topvpndeals.net/>what is vpn</a>
whats the best free vpn